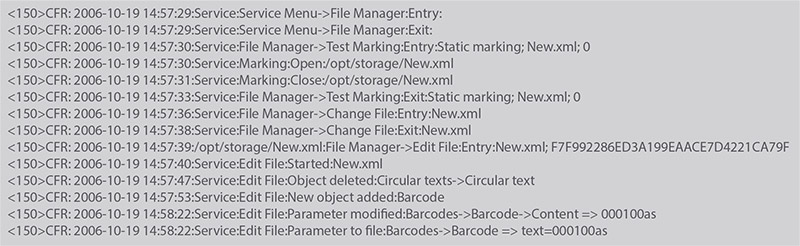
Jednoduše jde o uchování dat a dokumentů v podobě elektronického záznamu, kdy je generován většinou textový dokument, obsahující záznam o přihlášení do systému, provedené změny a následný provoz zařízení.
Jde o takový log-file, který má validitu díky zaheslovanému přístupu do systému.
Laser systém a FDA 21 CFR Part 11
Laserové systémy Solaris nabízí tyto volby pro splnění uvedených požadavků:
- Použití ovládání laseru v několika úrovních hesel a přístupů k ovládání
- Logging, nebo-li záznam všech aktivit uživatele s časovým údajem a uživatelskými změnami („Audit Trail“)
- Logging, nebo-li záznam všech systémových stavů s časovými údaji. Například chybové hlášení
- Rozšířený komunikační protokol pro integraci do zákaznické sítě s centralizovanou správou a uživatelskými daty (ERP systémy a například SAP R3)
- Datová bezpečnost via Windows XP Professional, NTFS souborový systém a nepřerušení napájení díky UPS
Historie FDA 21 CFR Part 11
Již v roce 1991 se podniky, jejichž výrobní program v USA podléhá státnímu (federálnímu) dozoru, začaly dotazovat FDA Amerického úřadu pro potraviny a léčiva (U.S. Food and Drug Administration – FDA)), jak a kdy by mohly namísto dokumentace vedené na papíře začít používat elektronické záznamy a tzv. elektronického podpisu.
Následovalo vydání směrnice FDA v srpnu roku 1997, zkráceně označovanou 21 CFR Part 11 (FDA: Part 11 of Title 21 of the Code of Federal Regulations: Electronic records; electronic signatures). Směrnice CFR 21 Part 11 stanovuje, že výrobní společnosti, jak z oboru farmacie, tak i potravinářství, mohou používat validitu elektronických záznamů a podpisy. Pro ty z nich, které při výrobě anebo distribuci výrobků podléhajících dozoru ze strany FDA (tzv. regulované produkty) používají počítačové systémy, je použití elektronických záznamů a podpisů doslova povinné. Směrnice 21 CFR Part 11 stanovuje procedury a technické požadavky, které jsou podmínkou použití počítačových systémů založených na elektronickém uchovávání dat a využívajících elektronický podpis. Určuje způsoby validace počítačového systému, autentizace uživatele, přístupu k systému a jeho zabezpečení, použití časových značek, uchovávání podkladů pro audit, příjmu záznamů a stanovuje, co je třeba především brát v úvahu při identifikaci požadovaného záznamu. Směrnice 21 CFR Part 11 je důležitá proto, že FDA, a spolu s ním pravděpodobně také další dohlížející úřady auditu a v neposlední řadě i mnozí vedoucí pracovníci v podnicích, budou uchovávat data v elektronické formě záznamu. Směrnice stanovuje, že elektronicky vytvořená výrobní data vyžadují inspekci auditu a elektronickou archivaci.
Jednoduchost implementace
Díky připravenosti zařízení na uvedenou normu shody s 21 CFR Part 11 jde o velmi levnou, finančně a administrativně nenáročnou implementaci, která významně neovlivní hospodaření firmy. Je zde zabezpečena přenositelnost dat a jejich snadná požadovaná archivace.
Budoucnost a 21 CFR Part 11
S růstem složitosti systémů pro automatizaci procesů používaných ve farmaceutické a potravinářské výrobě a současně s rostoucí angažovaností státních dohlížejících institucí, jako je např. FDA v USA, v oblasti validace počítačových řídicích systémů, je patrná potřeba určitého v praxi použitelného systému, jenž umožní tyto systémy specifikovat, konstruovat a validovat. Takovým systémem je směrnice FDA 21 CFR Part 11.
Norma u nás
U nás je dohlížejícím orgánem v oblasti farmacie Státní ústav pro kontrolu léčiv (SÚKL). Dále SÚKL konstatuje, že pokud by u nás měl výrobce elektronicky vedené záznamy o propuštění šarží (tj. včetně elektronických podpisů) a jeho počítačový systém by byl validován, pravděpodobně by nenarazil na problémy, a to také díky tomu, že v rámci EU zatím nebyl vydán žádný pokyn, který by toto detailně upravoval. Současná globální povaha výroby i spotřeby, ne tak zřídka přicházející proměny osvědčených nadnárodních, firemních apod. standardů ve všeobecně mezinárodně přijímané de facto standardy a v neposlední řadě i skutečnost, že někteří výrobci a dodavatelé již zmiňují směrnici 21 CFR Part 11 v souvislosti s vlastnostmi jimi nabízených produktů, nebrání produkci v rámci EU. Směrnice 21 CFR Part 11 v tento okamžik představuje metodu validace počítačových řídicích systémů v automatizované průmyslové výrobě, v principu ověřenou, mocně podporovanou a všeobecně dobře přijímanou.